Современное лечение гиперкоагуляционного синдрома
| ГИПЕРКОАГУЛЯЦИОННЫИ СИНДРОМ Понятие о гиперкоагуляционном синдроме (ГС) как об оригинальной самостоятельной форме патологии системы свертывания крови сформулировано А.И. Воробьевым в 1997 г. Наблюдение за пациентом с атероматозом коронарных сосудов, перенесшим хирургическое лечение (маммарное шунтирование) с развитием через неделю после операции коагулологических нарушений, позволило описать самостоятельную форму патологии гемостаза — ГС, провести четкую границу между ним и гиперкоагуляционной фазой ДВС-синдрома. Под ГС следует понимать коагулопатию, характеризующуюся определенными клиническими и преимущественно лабораторными признаками повышенного (ускоренного) свертывания крови при отсутствии образования тромбов. При ГС не наблюдается образования тромбов ни в артериальной, ни в венозной системе, ни в системе микроциркуляции. Однако при этом регистрируется состояние повышенной готовности циркулирующей крови к свертыванию. Патогенез. В основе формирования ГС лежит активация по тем или иным причинам механизмов свертывания крови при сохраненном сбалансированном противодействии противосвертывающих систем. Только в тех случаях, когда противосвертывающие механизмы сдерживают повышенную активность свертывающей системы крови, создаются условия формирования клинико-лабораторной картины ГС. Естественно, что при этом отсутствуют и признаки потребления факторов свертывания, нет и обязательного признака ДВС-синдрома — полиорганной патологии. Исходя из патофизиологических механизмов формирования и патогенетических особенностей течения в ГС можно выделить ряд специфических форм. 1. ГС при полиглобулии. Характеризуется избытком клеток в циркуляторном русле (типичный пример — эритроцитозы). что приводит к стазам крови преимущественно в системе микроциркуляции. 2. ГС при повреждении сосудистого эндотелия (эндотелиопатии). Наблюдается как при механическом его повреждении, так и при возникновении качественной неполноценности эндотелиальных клеток, что возможно при инфекциях, иммунокомплексной патологии, аутоиммунной агрессии, атеросклеротическом повреждении сосудистой стенки, токсических воздействиях и др. 3. ГС при гематогенных тромбофилиях. Часто сопровождается формированием тромбозов. Этот вариант ГС наблюдается при дефиците антитромбина III, аномалиях системы протеина С и протеина S, мутантном V факторе, мутации гена метилентетрагидрофолатредуктазы и гипергомоцистеинемии, мутантном протромбине, мутации интегрина, наличии волчаночного антикоагулянта — аутоантител к фосфолипидам, синдроме резко повышенной агрегации тромбоцитов — «липких тромбоцитах», существенном повышении уровня или мультимерности фактора Виллебранда и активности VIII фактора, высоком уровне XIII фактора. 4. ГС может формироваться при контакте крови с инородными поверхностями — искусственными клапанами сердца и протезированными сосудами, при проведении экстракорпорального очищения крови, операции с использованием аппарата искусственного кровообращения и др. 5. ГС, развивающийся при травматизации и разрыве сосудистой стенки, на первый взгляд, кажется необычным, так как при разрыве или повреждении сосудов обязательно формирование тромба. Однако при гемофилиях, болезни Виллебранда повреждение сосудов, по-видимому, может сопровождаться именно ГС, а не активным тромбозом. Поэтому у таких пациентов возможен быстрый переход ГС через короткую фазу гиперкоагуляции в гиперкоагуляционную фазу ДВС-синдрома. Кроме того, при наличии длительного локального кровотечения, наблюдающегося вследствие отсутствия полноценной остановки кровоточивости (язва желудка или двенадцатиперстной кишки, неспецифический язвенный колит и др.), «зияющие кровоточащие сосуды» всегда будут провоцирующим фактором быстрого перехода ГС в острый ДВС-синдром. 6. ГС может наблюдаться в качестве компенсаторного механизма при различного рода тромбоцитопе- нических синдромах (апластическая анемия, синдром Мошковиц и др.). 7. ГС при опухолях, прежде всего при прогрессировании ракового процесса. 8. ГС сопровождает трансформацию кровотока из ламинарного в турбулентный, что происходит при стенозировании сосудов (часто коронарных или других артерий), гемангиоматозе (гигантская гемангиома и др.). 9. ГС может развиться при эмоциональных стрессах, когда происходит выброс в циркуляторное русло катехоламинов. Этот вид ГС часто сочетается с его другими типами (при изменении характера кровотока, атеросклеротической эндотелиопатии, при гематогенных тромбофилиях, полиглобулиях и др.). 10. При исследовании у пациентов с ГС генетических мутаций выявлены гетерозиготные мутации V фактора и гомозиготные мутации гена протромбина. Полученные данные говорят о том, что при ГС, осложненном тромбофилией, необходимо исследование коагулологической системы крови как на молекулярном, так и на генетическом уровне. Последовательность коагулологических нарушений может быть схематически представлена следующим образом: первоначально имеющиеся различные варианты ГС при определенных условиях — падение артериального давления, кровотечение, обезвоживание и др. — переходят в гиперкоагуляционную фазу острого ДВС-синдрома, а иногда и в следующий этап — в гипокоагуляционную фазу острого ДВС-синдрома. Клиническая картина ГС неспецифична. Могут наблюдаться тяжесть в голове, иногда головные боли, признаки эмоциональной и психической заторможенности, быстрая утомляемость и слабость. Один из самых характерных симптомов — при взятии крови из вены она сворачивается в игле, а пунктированные вены быстро тромбируются и склерозируются. Диагностика и дифференциальная диагностика. Характерные клинические и лабораторные особенности ГС и фаз острого ДВС-синдрома представлены в табл. 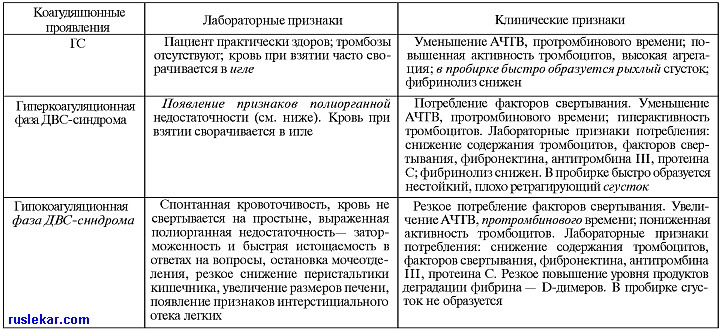 Острая массивная кровопотеря, сопровождавшаяся глубоким падением артериального давления и развитием стазов в системе микроциркуляции, практически всегда сопровождается гиперкоагуляционной фазой ДВС-синдрома. При эффективном лечении — переливании свежезамороженной плазмы, быстром восстановлении артериального давления — гиперкоагуляционная фаза острого ДВС-синдрома переходит в ГС. Лабораторно такой переход очень четко документируется устранением потребления факторов свертывания — обязательных и доказательных признаков ДВС-синдрома. Продолжительность ГС может быть различной. Лечение. Терапия ГС проводится с обязательным учетом его варианта и причин, приведших к его возникновению. Общими лечебными принципами являются применение различных комбинаций терапевтических средств и подходов: в/в введение (инфузоматом) нефракционированного гепарина; низкомолекулярные гепарины; непрямые антикоагулянты (cинкумар, пелентан и др.); сулодексид; антиагреганты (аспирин, тиклид, плавике); вазапростан; витамины В12, В6, фолиевая кислота; коринфар; никотиновая кислота. В определенных ситуациях назначают стероидные гормоны, цитостатики, плазмаферез и цитаферез. Терапия ГС является индивидуализированной и специфичной. При эритремии непосредственный избыток эритроцитов в циркуляторном русле необходимо устранить с помощью повторных сеансов эритроцитафереза. Гиперагрегабельность тромбоцитов требует назначения антиагрегантов (аспирин, тиклид), при наличии гиперкоагуляции проводят лечение низкомолекулярными гепаринами (фраксипарин, клексан или фрагмин/ По показаниям (прогрессия опухолевого роста) назначают цитостатики (гидроксимочевина и др.). В процессе эритроцитафереза пациенту вводят гепарин и назначают антиагреганты (преимущественно аспирин). ГС при первичном опухолевом гипертромбоцитозе (хронические миелопролиферативные заболевания) требует проведения терапии основного заболевания. Непосредственно гипертромбоцитоз с повышенной агрегационной активностью тромбоцитов лечится антиагрегантами (аспирин, плавике) и такими препаратами, как интерферон-а, гидроксимочевина, анаприлин. При ГС, развивающемся в ответ на повреждение эндотелия, терапия отличается многообразием. При инфекционной эндотелиопатии (сепсис, тяжелая пневмония, другие локальные инфекции) на фоне применения адекватных доз антибиотиков показано внутривенное (инфузоматом) введение нефракционированного гепарина. При патологии иммунных комплексов эффективны антиагреганты, низкомолекулярные гепарины и различные варианты плазмафереза. При аутоиммунной агрессии (системная красная волчанка и др.) наряду с использованием стероидных гормонов эффективна терапия гепарином, антиагрегантами, плазмаферезом. ГС при аутоиммунном венулите удается нивелировать путем сочетания внутривенного введения нефракционированного гепарина, процедур лечебного плазмафереза, назначения антиагрегантов (тиклид или плавике), стероидных гормонов (дексаметазон) и цитостатиков (винкристин, циклофосфан). ГС при атеросклеротическом повреждении сосудов (часто — коронарных артерий) наряду с традиционной терапией ИБС (нитраты, b-блокаторы, антагонисты кальция и др.) требует применения антиагрегантов (аспирин, тиклид, плавике), иногда их комбинаций (аспирин + плавике) в адекватных дозах: изучение агрегационных показателей тромбоцитов должно показать заблокированность агрегации тромбоцитов (отсутствие второй волны агрегации и наличие феномена дезагрегации тромбоцитов). Кроме того, пациенты должны получать терапию антикоагулянтами: предпочтение отдается пероральным препаратам — синкумар (непрямые антикоагулянты) или сулодексид (комплекс гликозаминогликанов). При остром ГС с угрозой развития тромбозов коронарных артерий и соответственно острого инфаркта миокарда необходимо внутривенное введение нефракционированного гепарина. Возможно использование препарата, представляющего собой специфические моноклональные антитела к мембранному гликопротеину IIЬ-IIIа тромбоцитов — Рео Про. Он не только позволяет резко оборвать гиперагрегабельность тромбоцитов и предотвратить тем самым развитие острого инфаркта миокарда, но и может благоприятно повлиять на характер дальнейшего течения ИБС. Терапия ГС при гематогенных тромбофилиях отличается специфичностью и разнообразием. При дефиците антитромбина III целесообразны периодические внутривенные введения очищенных препаратов антитромбина III, а при их отсутствии — переливание больших объемов свежезамороженной плазмы (1 — 1,5 л). Также проводится терапия антиагрегантами и непрямыми антикоагулянтами (синкумар, варфарин). При дефиците протеина С больным показаны переливания очищенных препаратов протеина С. В терапии ГС при гетерозиготном дефиците протеина С (протеин С является К-витаминзависимой протеазой, вырабатываемой в печени) лучше избегать назначения непрямых антикоагулянтов (синкумара, варфарина), так как эти препараты снижают не только активность в крови К-витаминзависимых факторов (VII, IX, X и XI факторов), но и уровень протеина С, что может усилить тромбогенность и привести к развитию так называемых варфариновых некрозов кожи. В этих ситуациях (при дефиците компонентов системы протеина С) предпочтительно использовать низкомолекулярные гепарины, комбинации антиагрегантов (например, аспирин + тиклид или аспирин + плавике). Гипергомоцистеинемический ГС лечится небольшими дозами витаминов B12, B6, а также фолиевой кислотой в дозе 5—10 мг/сут. Хорошие эффекты при гипергомоцистеинемии получают от плазмафереза. В терапии ГС при антифосфолипидном синдроме и наличии аутоантител волчаночного типа предпочтение отдается аспирину, низкомолекулярным гепаринам и повторным процедурам лечебного плазмафереза. При синдроме «липких тромбоцитов» необходимо добиться медикаментозной блокады функциональных параметров тромбоцитов. С этой целью применяют антиагреганты, часто их комбинации: аспирин + тиклид, аспирин + плавике. При помощи агрегатометрии добиваются феномена дезагрегации тромбоцитов в ответ на добавление ристоцетина и АДФ. При повышении уровней фактора VIII и фактора Виллебранда ГС купируется путем сочетания медикаментозных и экстракорпоральных методов терапии. Часто назначают низкомолекулярные гепарины или непрямые антикоагулянты (синкумар, варфарин), антиагреганты в сочетании с обычными или селективными методами плазмафереза. ГС при наличии контакта крови с инородными поверхностями лечится путем назначения адекватных доз непрямых антикоагулянтов (синкумар, варфарин) и антиагрегантов (аспирин, плавике). При применении экстракорпоральных методов очищения крови (гемодиализ, гемофильтрация, плазмаферез) или операций с использованием аппарата искусственного кровообращения для купирования ГС предпочтительны нефракцн- онированный или низкомолекулярные гепарины. ГС при травматизаиии и разрыве целостности сосудистой стенки в первую очередь требует остановки кровотечения, местного гемостаза, восстановления объема циркулирующей крови с помошью переливаний солевых и коллоидных растворов. Так как этот тип ГС легко переходит в гиперкоагуляционную фазу ДВС-синдрома, в его терапии преимущество отдается внутривенным трансфузиям достаточных объемов свежезамороженной плазмы. При тромботической тромбоцитопенической пурпуре для купирования ГС показаны периодические трансфузии свежезамороженной плазмы или криосупернатанта в сочетании с проведением процедур плазмафереза. Таким образом, лечение ГС основной целью имеет предупреждение перехода готовности к тромбозу в диссеминированное тромбообразование. Наиболее ярко такой переход демонстрирует токсикоз беременных, всегда сопровождающийся отчетливыми признаками ГС. ГС осложняется остро развивающейся полиорганной патологией и истечением из половых путей родильницы несвертывающейся крови. Это уже гипокоагуляционная фаза ДВС-синдрома, требующая быстрого вливания 2 л свежезамороженной плазмы (а не ампутации матки). | |
|
| |
| Просмотров: 10301 | |
| Всего комментариев: 0 | |